Actualización de la parvovirosis canina: diagnóstico y tratamiento.
Actualización de la parvovirosis canina: diagnóstico y tratamiento.
Resumen
La enteritis parvoviral canina es una de las causas más comunes de morbilidad y mortalidad en perros mundialmente. Ocasionada por el ADN virus del género Protoparvoviruscarnívoro 1 y 2 (PPC1 y PPC2); PPC1 afecta a perros de todas las edades, mientras que el PPC2 ha sido identificado como una de las causas principales de la enteritis hemorrágica viral en las crías caninas. El diagnóstico se realiza comúnmente a través de un ensayo por inmunoabsorción ligado a enzimas fecales (ELISA), sin embargo, no es la prueba más sensible y específica, por lo que en situaciones de falsos negativos se han investigado otros métodos diagnósticos, como los ensayos de reacción en cadena de la polimerasa (PCR). De cualquier manera, el pronóstico de la enfermedad es siempre reservado, ya que este depende de la carga viral, estado inmunológico del paciente, calidad del tratamiento, signos clínicos y evolución. El pronóstico además puede evaluarse obteniendo parámetros analíticos en los estudios de laboratorio.
El tratamiento principal es de soporte, que varía dependiendo de los signos clínicos del paciente. Asimismo, en los últimos años, han surgido terapias auxiliares con fármacos como el oseltamivir, interferón omega felino recombinante, plasma hiperinmune; y técnicas como el trasplante fecal, entre otras. Las cuales están siendo analizadas, esperando que en el futuro existan más opciones de tratamiento para los pacientes, mejorando su pronóstico.
Abstract
Canine parvoviral enteritis is one of the most common causes of morbidity and mortality in dogs worldwide. Caused by ADN virus of the genus carnivour Protoparvovirus 1 and 2, (CPPV 1 and CPPV 2); CPPV1 affects dogs of all ages, while CPPV2 has been identified as one of the principal causes of viral hemorrhagic enteritis on canine cubs. The common diagnosis is made through an enzyme-linked immunosorbent assay (ELISA), nevertheless, it is not the most specific and sensible test, hence in some situations of false negatives other methods of diagnostics have been investigated as Polymerase Chain Reaction essay (PCR). Either way the prognosis of this disease is always reserved, as it depends on the viral charge, inmunologic state of the patient, quality of treatment, clinical signs and evolution. Also the prognosis may be evaluated obtaining analytical parameters on laboratory studies.
The principal treatment is supportive, which may vary depending on the patient clinical signs. In addition, on the last years there have emerged new auxilary therapies with medicines like oseltamivir, recombinant feline interferon omega, hyperinmune plasma; and techniques as fecal transplant, among other things. The ones who are now being analyzed, hoping that more treatment options are aviable in the future for the patients, improving the prognosis.
Introducción y epidemiología
El parvovirus canino (PVC) de la especie Protoparvovirus carnívoro 1, género Protoparvovirus, subfamilia Parvovirinae, familia Parvoviridae, es un virus ADN monocatenario pequeño, sin envoltura, muy relacionado con el parvovirus felino (PVF), que en cánidos produce la parvovirosis canina. Esta es una de las enfermedades gastrointestinales víricas más importantes en perros jóvenes (N. Decaro, 2020). Descrita en los años 60 como tipo 1 (PVC-1) causante de enfermedad gastrointestinal y respiratoria en perros, mutando a la variante tipo 2 (PVC-2) en los años 70, la cual causó una pandemia tanto en perros jóvenes como en adultos y una década más tarde, en los años 80, se registraron otras dos variantes: PVC-2a y PVC-2b, seguida de una tercera variante en el año 2000: PVC-2c de distribución mundial (Mazzaferro, 2020). Estas variantes tipo 2 del parvovirus, son las responsables de la enfermedad como se conoce actualmente, aunque afecta principalmente a los perros domésticos, puede afectar también a otros mamíferos como: coyotes, lobos, gatos y mapaches (Mylonakis M, 2016).
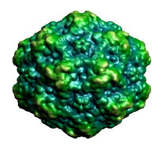
Ilustración 1. Imagen de la partícula viral de Parvovirus canino extraída del International Comittee of Taxonomy of Viruses
El virus puede estar presente en cualquier parte del medio ambiente, persistiendo desde 5 meses hasta 1 año, si se dan las condiciones ambientales favorables para que esto suceda (Jocelyn Mott, 2019). Las vías de infección principales son la oronasal, por contacto directo con fómites, vectores mecánicos (roedores o insectos); y heces de animales infectados (Bird, 2013), aunque también se ha documentado la vía transplacentaria, afectando a los recién nacidos (miocarditis) (A. Goddard, 2010).
Tras la infección con el virus, existe un periodo de incubación que puede oscilar entre los 4 y 14 días, durante el cual los perros, aunque permanezcan asintomáticos, pueden excretar el virus contagiando a otros cánidos (Mazzaferro, 2020; Mylonakis M, 2016). El virus se replica inicialmente y de manera autónoma en tejido orofaríngeo, linfonodos y timo, produciendo luego un período de viremia, que dura de 1 a 5 días (A. Goddard, 2010). Posteriormente, las células entéricas en división son infectadas, médula ósea, epitelio de la lengua, cavidad oral y miocitos cardiacos; en adición a pulmones, bazo, hígado y riñones (J. Ford, 2017; Mazzaferro, 2020). Como consecuencia de la infección, aparece leucopenia significativa, seguida de gastroenteritis hemorrágica y emesis, progresando y predisponiendo a sepsis, fallo multiorgánico por translocación bacteriana intestinal, síndrome de respuesta inflamatoria sistémica (SRIS); y shock hipovolémico. Lo que lleva al fallecimiento del paciente (Mazzaferro, 2020; N. Decaro, 2020).
Diagnóstico
Los hallazgos más comunes en el hemograma son: leucopenia por neutropenia y linfopenia. La linfopenia puede ocurrir tanto en cachorros infectados por PVC, como en otras enfermedades como la salmonelosis o el coronavirus. Dicha leucopenia refleja la respuesta inmunitaria del animal, y ayuda a predecir el desenlace de la enfermedad: se observó que el mantenimiento del recuento total de leucocitos por encima de 4500 / ml y de linfocitos mayor a 1000 / ml en la admisión del paciente y durante las primeras 48 horas de hospitalización fueron grandemente predictivas de la supervivencia del mismo (Jocelyn Mott, 2019; A. Goddard, 2010; Sykes, 2014; Mazzaferro, 2020). Otras alteraciones frecuentes son: anemia regenerativa moderada, trombocitopenia o trombocitosis, leucocitosis neutrofílica o monocitosis y en algunas ocasiones pancitopenia grave. En el frotis sanguíneo es común observar neutrófilos con signos de toxicidad la vacuolización espumosa por formación anómala de lisosomas y liberación en la célula de enzimas autolíticas, la granulación tóxica que consiste en presenciar la granulación rosa típica del neutrófilo la cual debería haber perdido en el proceso de maduración, el gigantismo celular que se produce por la falta de divisiones mitóticas en el proceso de desarrollo de estas células y, como último signo grave de toxicidad neutrofílica que se podría dar en el desarrollo de esta enfermedad, es la presencia del núcleo en anillo (Mazzaferro, 2020; A. Goddard, 2010; Sykes, 2014) Realizar perfiles bioquímicos y gasometrías ayudan a evaluar el estado ácido-básico del paciente y si hay cambios asociados a daño en órganos diana. La parvovirosis canina puede causar distintas alteraciones, siendo las más frecuentes la acidosis metabólica con hiperlactatemia, la hipopotasemia, la hipoglucemia y la hipoproteinemia por hipoalbuminemia. Además de estas, se pueden observar otros cambios analíticos como: azotemia, panhipoproteinemia, hiperglucemia, hipomagnesemia, hiponatremia, hipocloremia e hiperbilirrubinemia (Mazzaferro, 2020) (Jocelyn Mott, 2019) (Sykes, 2014). La hipoglucemia también es común en los cachorros jóvenes y puede estar asociada a desnutrición grave, malabsorción, deficiencia de reservas de glucógeno hepático y muscular y/o septicemia. Todo ello puede provocar una neuroglucopenia generando convulsiones secundarias, por tanto, la glicemia es un parámetro muy importante que debe ser monitorizado y corregido rápidamente si se identifican hipoglicemias (Mylonakis M, 2016; A. Goddard, 2010; Mazzaferro, 2020; Sykes, 2014). Aunque, hay que tener en consideración que en los estados de sepsis y shock se pueden presentar hiperglicemias asociadas (Torre DM, 2007). El PVC también puede producir alteraciones de la hemostasia, como consecuencia de un síndrome de respuesta inflamatoria sistémico o sepsis y daño al glicocalix, las cuales se pueden identificar con la realización de una tromboelastografía, tiempos de coagulación y medición de concentración de fibrinógeno en plasma, entre otras pruebas (Mazzaferro, 2020; Sykes, 2014). Entre los más comunes se encuentran: aumento de la amplitud máxima de la tromboelastografía, un aumento del tiempo de tromboplastina parcial activada, un aumento de la concentración de fibrinógeno y una disminución de la actividad de la antitrombina (Mazzaferro, 2020).
Por otro lado, aunque menos comunes en estos casos, se encuentran los estudios de imagen (radiología y ultrasonografía abdominal), donde se pueden observar algunos cambios (inespecíficos) asociados a esta patología, donde se suele observar asas intestinales con líquido o gas, hiper o hipomotilidad, adelgazamiento de la mucosa, linfadenopatía, etcétera. Estas pruebas son utilizadas principalmente para descartar diferenciales de enfermedades que comparten la misma signología que PVC (ej. evaluar la presencia de un cuerpo extraño, pancreatitis, perforación gastrointestinal etc.), e igualmente, pueden ser auxiliares para identificar complicaciones debidas a hipermotilidad (ej. Intusucepción intestinal) o hipomotilidad (Mazzaferro, 2020; Jocelyn Mott, 2019).
as pruebas específicas para confirmar el diagnóstico de PVC son realizadas por medio de: hemaglutinación, ELISA, PCR, microscopía electrónica, histopatología o aislamiento del virus (A. Goddard, 2010; Mazzaferro, 2020; Sykes, 2014). La prueba de hemaglutinación para el diagnóstico del PVC es un método serológico que consiste en la combinación del virus con anticuerpos específicos, con el fin de evaluar el título de anticuerpos presentes (Bird, 2013; Sykes, 2014). Esta prueba es poco sensible, y requiere muestras frescas, por ello es poco empleada.
El método más común de detección de la enfermedad, debido a que se trata de una prueba rápida y de bajo coste, puede ser realizada dentro de la misma clínica veterinaria, y tiene un costo accesible, es un ELISA inmunocromatográfico de heces o contenido intestinal, el cual posee elevada sensibilidad (cercana al 100%), aunque su especificidad puede ser de mediana a baja, comparándola con métodos como el PCR (N. Decaro C. V., 2020; N. Decaro C. B., 2012). Es importante que las muestras de heces sean frescas. Estas muestras deben tener 106 copias de ADN por
Ilustración 2. Paciente diagnosticado con parvovirosis canica.
miligramo de heces como mínimo para obtener un resultado positivo. Si hay un alto número de anticuerpos frente al PVC en el tracto gastrointestinal, estos se unen al virus formando inmunocomplejos de manera que el test ELISA no detectará al antígeno libre, dando un resultado falso negativo (Mylonakis M, 2016; Proksch, 2015). Otra causa para un falso negativo, es realizar la prueba al inicio de la enfermedad, donde la diseminación viral es baja. Mientras que la inmunización previa con vacunas vivas atenuadas puede arrojar un falso positivo (Bird, 2013). Por lo tanto, el método más sensible (80-100%) y específico (100%) para el diagnóstico de la enfermedad es por medio de PCR (Mazzaferro, 2020).
Uno de los principales retos en los centros veterinarios es convencer al dueño de mantener hospitalizado a su perro, por el costo que implica. Ya que pueden pasar desde 3 días hasta 1 mes en terapia intensiva (dependiendo del caso).
El tratamiento para la parvovirosis canina es de soporte hasta que los signos clínicos se hayan resuelto. En general, esto corresponderá a un aumento marcado del conteo leucocitario; no obstante, el desarrollo de secuelas como neumonía por broncoaspiración, hipoglicemia o hiperglicemia, hipoalbuminemia con edema, o intususcepción incrementan el tiempo de hospitalización y posible muerte (Mazzaferro, 2020).
Uno de los manejos más eficaces, pero más agresivos, es la administración de terapia de líquidos cristaloides isotónicos por medio de un catéter endovenoso. El volumen inicial dependerá del estado del paciente, si este presenta signos de hipovolemia (taquicardia, bradicardia, hipotermia, tiempo de llenado capilar retardado, hipotensión) será necesario administrar bolos de 20ml/kg, tan pronto como sea posible (manteniendo monitoreo en la perfusión) para incrementar el volumen vascular, reponer pérdidas entéricas y mantener la hidratación del paciente (Mazzaferro, 2020). Esta terapia se recomienda reajustar con el requerimiento personalizado de cada paciente, durante 12-24 horas, según la evolución y respuesta del paciente (Bird, 2013; Mylonakis M, 2016; Mazzaferro, 2020). Una forma de monitorear la respuesta en cuanto a hidratación es pesar constantemente al paciente, ya que 1g de peso corporal es equivalente a 1ml de líquidos perdidos (Mazzaferro, 2020).
Tratamiento
Para complementar el tratamiento, se recomienda el uso de medicamentos sintomáticos y nuevas alternativas como: antivirales (oseltamivir), interferón omega felino recombinante, plasma hiperinmune, factor estimulante de granulocitos, antieméticos y protectores gástricos, además de proveer analgesia multimodal, garantizar la micronutrición del enterocito y regular los niveles de glucemia; todo esto, sin olvidar prevenir infecciones secundarias con el uso responsable de antibióticos, ya que esto puede comprometer aún más al paciente hospitalizado (Mazzaferro, 2020; Mylonakis M, 2016). Otra herramienta para considerar es el transplante de microbiota fecal, el cual consiste en administrar rectalmente 10g de heces de un paciente sano, diluido en 10ml de suero fisológico estéril (0.9%). Este tratamiento tiene beneficios multipropósito, incluyendo: función de barrera protectora, nutrición para el enterocito, regulación de la inmunidad; y motilidad intestinal. Está documentado que los pacientes que han recibido el transplante fecal han tenido mayor tasa de supervivencia (G.Q. Pereira, 2018).
Prevención
Una de las formas de prevenir y reducir las infecciones por parvovirus, es la higiene y limpieza de las zonas compartidas entre caninos, como clínicas veterinarias, pensiones, escuelas de adiestramiento, etc. Se puede utilizar hipoclorito de sodio diluido al 0.75%. aplicándolo en superficies para eliminar al virus y así evitar su diseminación. La única manera de evitar al 100% el contagio, es aislar al animal de cualquier zona contaminada con el virus, así que es prácticamente imposible; ya que aún los adultos bien inmunizados pueden contraerlo y diseminarlo (como portadores asintomáticos) (Mazzaferro, 2020). En adición, la forma más eficaz de evitar la infección y enfermedad por PVC, es por medio de la inmunización de las mascotas. Los cachorros de 6 a 16 semanas son los más vulnerables, en cuanto la inmunidad materna comienza a disminuir (8 semanas -12 semanas) incrementará el riesgo de infección. Por lo tanto, es imperativo comenzar con la vacunación para estimular la inmunidad innata. Los protocolos sugieren el uso de vacunas vivas modificadas, comenzando a las 6 semanas, repitiendo la inmunización cada 3 a 4 semanas, hasta las 16 semanas. Por otro lado, para los perros con alta exposición (ej. refugios), la vacunación puede ir desde las 4 semanas, hasta las 20 semanas de vida (K.G. De Cramer, 2011).
A. Goddard, A. L. (2010). Canine Parvovirus. Veterinary Clinics of North America: Small Animal Practice, 1041-1053.
Bird, L. &. (2013). Canine parvovirus: Where are we in the 21st Century? Companion Animal, 142-146.
D. Purvis, R. K. (1994). Systemic Inflamatory Response Syndrome: septic shock. Veterinary Clinics of North America: Small Animal Practice., 1225-1247.
G.Q. Pereira, L. G. (2018). Fecal microbiota transplantation in puppies with canine parvovirus infection. Journal of Veterinary Internal Medicine, 707-711.
J. Ford, L. M. (2017). Parvovirus infection is associated with myocarditis and myocardial fibrosis in young dogs. Veterinary Pathology, 964-971.
Jocelyn Mott, J. A. (2019). Blackwell’s Five-Minute Veterinary Consult Clinical Companion: Small Animal Gastrointestinal Diseases. En J. A. Jocelyn Mott, Blackwell’s Five-Minute Veterinary Consult Clinical Companion.(págs. 337-344). John Wiley & Sons.
K.G. De Cramer, E. S. (2011). Efficacy of vaccination at 4 and 6 weeks in the control of canine parvovirus. Veterinary Microbiology, 126-132.
L.M. Strom, J. R. (2015). Parvoviral Myocarditis in a dog.Journal of American Veterinary Medicine Association, 853-855.
Mazzaferro, E. M. (2020). Update on Canine Parvoviral Enteritis. Veterinary Clinics of North America: Small Animal Practice, 1307-1325.
Mylonakis M, K. I. (2016). Canine parvoviral enteritis: an update on the clinical diagnosis, treatment, and prevention. Vet Med (Auckl), 91-100.
N. Decaro, C. B. (2012). Canine parvovirus – A review of the epidemiological and diagnostic aspects, with emphasis on type 2c. Veterinary Microbiology, 1-12.
N. Decaro, C. V. (2020). Canine parvovirus vaccination and immunisation failures: Are we far from disease eradication. Veterinary Microbiology.
Proksch, A. L. (2015). Influence of clinical and laboratory variables on faecal antigen ELISA results in dogs with canine parvovirus infection. The Veterinary Journal, 304-308.
Sykes, J. E. (2014). Canine Parvovirus Infections and Other Viral Enteritides. Canine and Feline Infectious Diseases, Elsevier., 141-151.
Torre DM, d. A. (2007). Incidence and clinical relevance of hyperglycemia in critically ill dogs. Journal of Veterinary Internal Medicine.
Referencia ilustración 1. http://www.ictvonline.org
Referencia ilustración 2. Propiedad del Autor.








